科学研究 | mRNA 精准递送新突破!中大药学院(深圳)团队攻克胶质瘤治疗难题
近日,中山大学药学院(深圳)邓文斌教授、邓冠军副教授团队在国际知名期刊《Nature Communications》(IF=16.6)发表题为 “mRNA vaccine developed for sequential selective organ-to-cell targeting of glioma” 的高水平研究论文,成功突破 mRNA 药物肝脏富集的递送瓶颈,构建出具备双层精准递送能力的胶质瘤 mRNA 疫苗,为中枢神经系统肿瘤的免疫治疗提供了全新策略与技术支撑。我院硕士研究生石琳、李悦楹为该研究共同第一作者,邓文斌教授、邓冠军副教授为通讯作者。相关研究得到深圳市重点实验室、广东省自然科学基金、深圳市科技计划、广东省基础与应用基础研究基金等多个项目的资助。
mRNA 疗法是生物医药领域的研究前沿,在疫苗、肿瘤免疫治疗等方向展现出巨大临床潜力,然而系统给药的脂质纳米颗粒(LNP)易富集于肝脏,肝脏外器官与特定细胞的精准递送难题,成为制约 mRNA 药物临床转化的核心障碍。传统配体修饰策略又存在制备复杂、稳定性不足等缺陷,亟需全新的递送技术解决方案。
针对这一关键科学问题,邓文斌、邓冠军团队自主合成 meta/ortho/para 三类构型的可电离脂质,构建了不含 PEG 脂质的三组分脂质纳米颗粒(tLNP),并创新性提出Sequential Selective Organ-to-Cell Targeting(SSOCT)序贯性器官——细胞靶向策略,实现了 mRNA 从脾脏到树突状细胞(DC 细胞)的双层精准递送,完美规避了肝脏富集的问题。基于该策略,团队以 meta-tLNP 递送胶质瘤特异性突变抗原 IDH1 R132H mRNA,成功构建胶质瘤疫苗(mXO10 tLNP@mIDH1)。该疫苗在小鼠模型中展现出强效的抗肿瘤能力,单药即可有效抑制胶质瘤生长,与Anti-PD-1免疫检查点抑制剂联合使用时,更实现了肿瘤的彻底清除,为胶质瘤的临床治疗提供了极具转化价值的新方案。
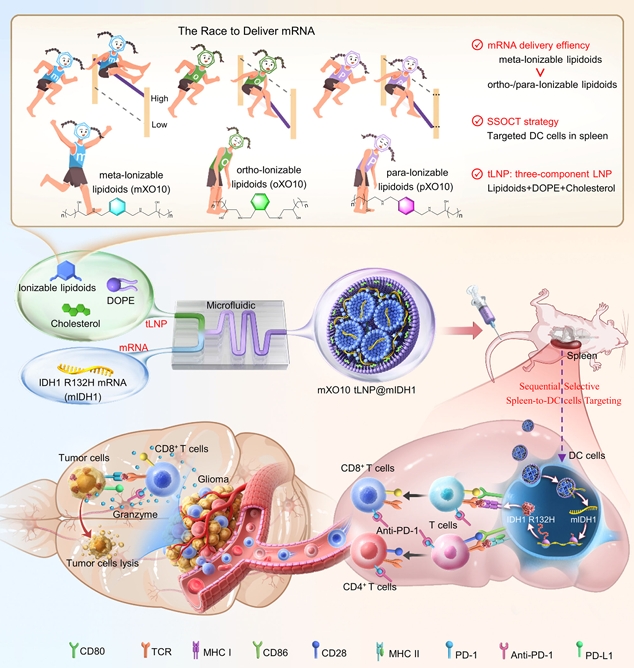
图1. 构建了由meta/ortho/para三类构型的可电离脂质所构建的三组分tLNP,实现“先脾脏、再树突状细胞”的 SSOCT 精准递送,并利用meta‑tLNP递送 IDH1 R132H mRNA 构建疫苗,在小鼠中有效清除胶质瘤并与Anti-PD-1协同增强疗效。
此项研究的顺利开展,依托于团队在mRNA精准递送、纳米医学、中枢神经系统疾病治疗等领域的深厚研究积淀与跨学科协作能力。团队核心成员邓文斌教授与邓冠军副教授在各自研究方向深耕多年,带领团队持续攻坚生物医药前沿难题,形成了从基础研究到技术转化的完整研究体系。
邓文斌教授,中山大学药学院(深圳)院长,加州大学戴维斯分校终身教授,“广东省干细胞与创新药物工程技术研究中心”主任。先后毕业于第二军医大学、北京协和医学院、美国罗格斯大学,并在哈佛大学医学院完成博士后研究,2016年加盟中山大学。长期致力于干细胞与胶质细胞生物学及其中枢神经再生的基础与应用研究,在该领域取得多项创新性成果,发表高水平论文180余篇,研究成果发表于《Nature Communications》《Cell Reports》等国际顶级期刊,为中枢神经系统损伤与退行性疾病的治疗奠定了重要理论基础,搭建了先进技术路径。
邓冠军副教授,中山大学药学院(深圳)“百人计划” 引进人才,深圳市 “鹏城孔雀计划” C 类人才、光明区高层次人才,广东省干细胞与创新药物工程技术研究中心等平台核心成员。长期聚焦mRNA精准递送、体内细胞编辑、细胞与基因治疗前沿研究方向,重点开展缺血性脑卒中、多发性硬化症、脑胶质瘤等中枢神经系统疾病的转化医学探索。主持国家自然科学基金、广东省自然科学基金等多项科研课题,以第一或通讯作者在《Nature Communications》《Advanced Materials》《ACS Nano》等国际顶级期刊发表系列成果,累计申请国家发明专利10余项,2项已成功转化,同时担任多个国际期刊青年编委及审稿人,在纳米医学与mRNA治疗技术领域具有重要学术影响力。
目前,邓文斌、邓冠军团队正围绕mRNA精准递送、细胞与基因治疗、中枢神经系统疾病创新药物研发等方向开展深度研究,现有多个在研项目处于关键阶段,科研平台完善、经费充足、合作资源丰富。为进一步壮大研究团队,推动更多前沿成果从实验室走向临床,现面向全球诚聘博士后研究人员,欢迎在生物医学工程、纳米材料、药剂学、分子生物学、肿瘤免疫学、干细胞生物学等相关领域具有扎实研究基础和创新思维的优秀青年学者加盟。
项目联系人:邓冠军老师
联系邮箱:denggj3@mail.sysu.edu.cn



