科学研究|我院陈建伟青年研究员团队在Advanced Science上发表研究论文
研究背景
蛋白水解靶向嵌合体(PROTACs)是一种不同于传统“占据驱动”模式的新兴靶向蛋白降解技术,开创了“事件驱动”的药理新范式。与传统小分子药物依靠可逆性占据靶点活性位点来抑制功能不同,该分子一端结合靶蛋白,另一端招募E3泛素连接酶,促使两者靠近并形成三元复合物,进而引导靶蛋白被泛素化标记并被蛋白酶体彻底水解。PROTACs分子在此过程中可循环使用,表现出催化特性。该技术能够克服传统“不可成药”靶点的限制,并通过完全清除靶蛋白来规避某些耐药机制。然而,该领域的发展仍面临关键瓶颈:PROTACs技术虽前景广阔,但严重受限于可用的E3连接酶,在超过600种人类E3连接酶中,仅有VHL、CRBN和XIAP等少数被成功应用于靶向蛋白降解(TPD)。
研究内容
近期,我院陈建伟青年研究员团队在期刊《Advanced Science》上发表了一项题为“Discovery of SKP2-Recruiting PROTACs for Target Protein Degradation”的研究。该研究聚焦于CRL1 E3连接酶的底物受体蛋白SKP2,在已知配体基础上通过设计优化,获得了化合物SL1。经分子对接及生物物理实验(SPR和CETSA等)验证,SL1能以中等亲和力结合SKP2,并成功转化为PROTACs中的E3连接酶招募模块。研究进一步将SL1与不同靶蛋白配体连接,证明了基于SKP2的PROTACs能有效诱导BRD4蛋白和雄激素受体(AR)蛋白的降解。
本研究首次将CRL1家族的SKP2引入TPD领域,显著扩充了可用于TPD的E3连接酶库,为发展具有组织选择性、可能规避耐药的新型降解剂提供了新的思路与策略。
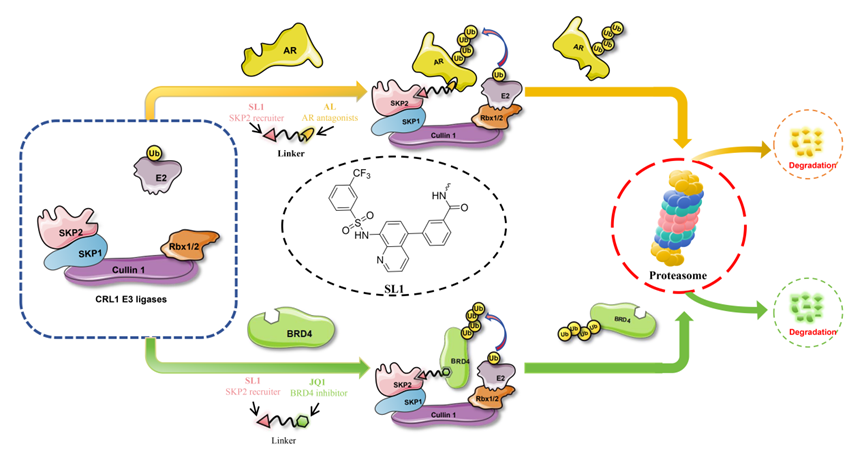
图1. 基于靶向SKP2的配体SL1,通过连接子将其分别与BRD4抑制剂JQ1或AR拮抗剂AL连接,设计非共价PROTAC分子,成功诱导BRD4和AR的泛素化及后续蛋白酶体降解。
通讯作者介绍
陈建伟,中山大学药学院(深圳)“百人计划”青年研究员、博士生导师,深圳市鹏城特聘教授。2012年博士毕业于中国科学院上海有机化学研究所,随后赴美国贝勒医学院药理学与化学生物学系从事博士后研究,历任研究助理、助理教授;2022年5月加入中山大学药学院(深圳)。
陈建伟课题组长期深耕于药物化学与化学生物学前沿交叉领域,聚焦抗体偶联药物(ADC)与靶向蛋白降解(TPD)策略,形成了鲜明的研究特色。团队在前期研究中奠定了坚实的方法学基础,课题组近年来着力于新型蛋白降解平台的拓展,并在E3连接酶的新应用研究中取得突破:首次证实SKP2可作为PROTAC的有效招募端,成功构建了基于该新型连接酶的靶向降解剂。相关成果发表于 Adv. Sci.、Angew. Chem. Int. Ed.、J. Am. Chem. Soc.、Nat. Commun.、PNAS 等国际权威期刊,并申请多项国际发明专利。团队坚持以关键技术突破驱动创新药物发现,致力于为靶向治疗策略的开发提供新思路与新工具。
论文信息
参考文献:
Guanjun Dong, Aima Huang, Ziqing Zhao, Bikai Lai, Xin Pan, Huiyu Yang, Xiaohan Xu, Tianwei Wang, Fangchen Zhao, Zhimin Zhang, Yongbo Xue, Guanjun Deng, Wenbin Deng, Jianwei Chen. Discovery of SKP2-Recruiting PROTACs for Target Protein Degradation. Adv Sci (Weinh). 2026 Feb 4: e15159.
文章链接:
https://doi.org/10.1002/advs.202515159



